4. các khía cạnh sinh lý bệnh và di truyền hướng dẫn điều chỉnh
4. các khía cạnh sinh lý bệnh và di truyền hướng dẫn điều chỉnh
4.1 Khuynh hướng di truyền
AF, đặc biệt AF khởi phát sớm, có thành phần di truyền mạnh mẽ, độc lập của các trạng thái tim mạch đi kèm. Một vài bệnh nhân AF trẻ bị các bệnh cơ tim qua trung gian các đột biến gây bệnh. Những bệnh đơn gene này cũng di truyền nguy cơ đột tử (xem Chương 6). Lên đến 1/3 các bệnh nhân AF mang các biến thể di truyền phổ biến dẫn đến AF, mặc dù với một nguy cơ gia tăng tương đối thấp.
Ít nhất 14 trong số các biến thể phổ biến, thường đa hình thái nucleotide đơn, được biết làm tăng nguy cơ xuất hiện AF. Các biến thể quan trọng nhất được đặt gần gene cặp giống như yếu tố phiên mã homeodomain 2 (Pitx2) trên nhiễm sắc thể 4q25. Những biến thể làm thay đổi các nguy cơ AF lên đến bảy lần. Một số biến thể nguy cơ AF cũng liên quan với tắc nghẽn tim mạch hoặc đột quỵ thiếu máu cục bộ, có thể do AF im lặng (xem chương 5 và 5.2) . Các thay đổi trong đặc tính điện thế hoạt động nhĩ, tái cấu trúc nhĩ, cũng như thâm nhập của các khiếm khuyết gene hiếm được sửa đổi đã được gợi ý như cơ chế tiềm tàng làm trung gian cho nguy cơ AF tăng lên ở những người mang các biến thể gene thông thường. Biến thể di truyền có thể, trong tương lai, trở thành hữu ích cho lựa chọn bệnh nhân kiểm soát nhịp hoặc kiểm soát tần số. Trong khi phân tích bộ gene có thể cung cấp cơ hội để cải thiện chẩn đoán và điều chỉnh AF trong tương lai, xét nghiệm di truyền thường xuyên cho các gen thông thường biến thể kết hợp với AF không được khuyến cáo hiện thời.
4.2 Các cơ chế đưa đến rung nhĩ
4.2.1 Tái cấu trúc cấu trúc nhĩ và chức năng kênh ion
Những căng thẳng bên ngoài chẳng hạn như bệnh tim cấu trúc, tăng huyết áp, có thể bệnh tiểu đường, nhưng cũng tự bản thân AF tạo ra một quá trình tái cấu trúc trong nhĩ chậm nhưng tiến triển (Hình 2). Kích hoạt các nguyên bào sợi, lắng đọng mô liên kết gia tăng, xơ hóa là điểm nổi bật của quá trình này.[78-80] Ngoài ra, thâm nhiễm mỡ trong nhĩ, thâm nhiễm viêm, phì đại tế bào cơ, hoại tử và amyloidosis được tìm thấy ở những bệnh nhân AF với điều kiện đồng thời mở đường cho AF. Tái cấu trúc gây ra phân ly điện học giữa các bó cơ và mất sự đồng nhất dẫn truyền khu vực, thúc đẩy vào lại và duy trì rối loạn nhịp . Ở nhiều bệnh nhân, tiến triển tái cấu trúc thực thể biểu hiện trước khởi phát AF. Ở một số tái cấu trúc thực thể sẽ không thể phục hồi, khởi đầu điều trị sớm dường như thất bại. Bảng 4 đưa ra một tổng quan về các thay đổi sinh bệnh lý liên quan phổ biến trong tổ chức nhi kết hợp với AF, cả một danh sách tương ứng với các điều kiện lâm sàng có thể đóng góp vào những thay đổi này.
Bảng 4.Các thay đổi sinh lý bệnh trong tổ chức nhĩ kết hợp với rung nhĩ và các trạng thái lâm sàng có thể đóng góp vào sự thay đổi như vậy
|
Các thay đổi sinh lý bệnh |
Các trạng thái lâm sàng đóng góp vào sự thay đổi |
Cơ chế thúc đẩy loạn nhịp/hậu quả chức năng. |
Tài liệu tham khảo |
|
Các thay đổi của môi trường bên ngoài tế bào, chức năng tế bào sợi, tế bào mỡ. |
|||
|
Sơ tổ chức kẽ và thay thế sợi |
AF (đặc biệt hình thái với gánh nặng AF cao), THA, HF, bệnh van tim (do quá tải thể tích và áp lực) |
Phân ly điện học, block dẫn truyền, biến chứng AF gia tăng |
78,79,90,91 |
|
Thâm nhiễm viêm |
|
Đáp ứng thúc đẩy xơ, biến chứng AF gia tăng. |
81 |
|
Thâm nhiễm mỡ |
Béo phì |
Đáp ứng thúc đẩy xơ / viêm, block dẫn truyền khu vực |
82, 92 |
|
Lắng đọng amyloide |
Tăng tuổi, HF, bệnh động mạch vành (do sẹo nhĩ, các yếu tố di truyền) |
Rối loạn dẫn truyền |
83, 93 |
|
Các thay đổi kênh ions |
|||
|
Tái cấu trúc kênh ions |
AF (đặc biệt hình thái với gánh nặng AF cao), các khuynh hướng di truyền đưa đến AF |
Vòng AF ngắn lại (nếu do nhịp nhanh nhĩ), kéo dài chiều dài vòng AF (nếu do HF), không đồng nhất tái cực nhĩ gia tăng. |
94, 96 |
|
Ca++ xử lý không ổn định. |
AF (Hình thái đặc biệt với gánh nặng AF), HF, THA (có thể qua hoạt động giao cảm gia tăng) |
Xu hướng ngoại vị gia tăng |
97, 98 |
|
Tái phân phối lại các nối khoảng trống. |
AF |
Rối loạn dẫn truyền |
99 |
|
Thay đổi tế bào cơ |
|||
|
Chết theo chương trình và hoại tử |
Bệnh động mạch vành, HF (chuyển qua chết tế bào cơ tim và sẹo nhĩ) |
Có thể tạo ra sợi thay thế |
100 |
|
Phì đại tế bào cơ |
Giãn nhĩ, AF |
Thúc đẩy rối loạn dẫn truyền |
84, 101 |
|
Thay đổi nội mạc và mạch máu |
|||
|
Các thay đổi mạch máu lớn |
Vữa xơ, bệnh mạch động mạch vành và ngoại biên, có thể AF |
Thúc đẩy thiếu máu cục bộ nhĩ, không đồng nhất chức năng điện học, tái cấu trúc thực thể. |
102 |
|
Tái cấu trúc nội tâm mạc |
|
Nguy cơ hình thành huyết khối gia tăng |
103,104 |
|
Các thay đổi hệ thống thần kinh tự động |
|||
|
Cường chức năng chi phối giao cảm |
HF, THA |
Xu hướng ngoại vị gia tăng |
80,105 |
AF: rung nhĩ. HF: suy tim. THA: tăng huyết áp.
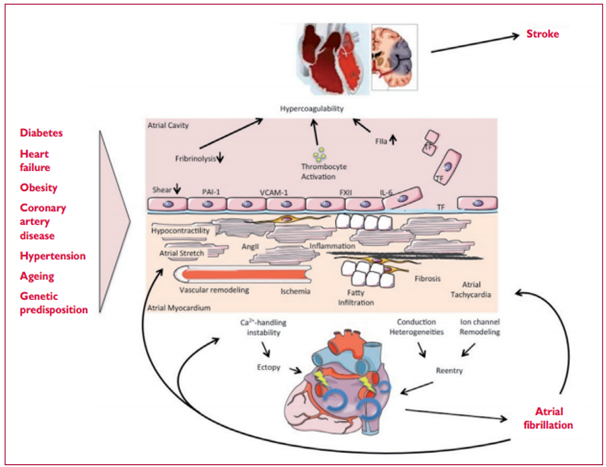
Hình 2.Các cơ chế gây rung nhĩ.
Stroke: đột quỵ. Diabetes: tiểu đường. Heart failure: suy tim. Obesity: béo phì. Coronary artery disease: bệnh động mạch vành. Hypertension: tăng huyết áp. Ageing: tuổi già. Genetic predisposition: khuynh hương di truyền. Atrial fibrillation: rung nhĩ. Atrial cavity: khoang nhĩ. Fibrinolysis: tiêu sợi huyết. Hypercoagulability: tăng đông máu. Thrombocyte activity: hoạt hóa tiểu cầu. Hypocontractility: giảm co thắt. Atrial stretch: căng nhĩ. AngII: angiotensin II. Imflammation: viêm. Vascular remodeling: tái cấu trúc mạch. Ischemia: thiếm máu cục bộ. Fatty infiltration: thâm nhiễm mỡ. Fibrosis: xơ hóa. Atrial tachycardia: nhịp nhanh nhĩ. Atrial myocardium: cơ tim nhĩ. Ca++handing instability: Trao đổi ion canxi bất ổn. Conduction heterogeneity: không đồng nhất dẫn truyền. Ion channel remodeling: tu sửa kênh ion. Ectopy: ngoại vị. Reentry: vào lại.
Hình 2 mô tả các cơ chế chính gây rung nhĩ có thể được xem xét khi lựa chọn điều trị. Các yếu tố bệnh căn khác nhau (trái) gây ra một danh sách phức tạp các thay đổi sinh lý bệnh trong nhĩ, gồm cả dầy lên và xơ sẹo (xơ hóa) gây ra do căng giãn nhĩ, giảm co bóp, thâm nhiễm mỡ, viêm, tái cấu trúc mạch máu, thiếu máu cụ bộ, rối loạn chức năng kênh ion, cũng như mất ổn định Ca2+. Những thay đổi này gia tăng các ngoại vị và rối loạn dẫn truyền, làm tăng xu hướng nhĩ để phát triển hoặc duy trì AF. Đồng thời, một số những thay đổi này được tham gia vào sự xuất hiện của trạng thái tăng đông có liên quan với AF. Ví dụ, co bóp giảm làm giảm căng nội mạc đan xen khu vực, trong đó tăng áp lực PAI-1, cả viêm do thiếu máu cục bộ làm gia tăng áp lực các phân tử kết dích nội mạc hoặc làm rối loạn sự bong các tế bào nội mạc, dẫn đến bộc lộ yếu tố tổ chức với dòng máu. Các thay đổi này bổ xung vào môi trường tạo đông máu trong nhĩ ở bệnh nhân AF. AF tự bản thân có thể làm trầm trọng thêm nhiều cơ chế đã được biết, trong đó có thể giải thích bản chất tiến triển của rối loạn nhịp.
Những thay đổi cấu trúc và chức năng trong cơ nhĩ và ứ máu, đặc biệt ở tiểu nhĩ (left atrial appendage: LAA), tạo ra một môi trường thúc đẩy đông máu. Hơn nữa, thậm chí các cơn AF ngắn cũng đưa đến tổn thương nhĩ và bộc lộ các yếu tố thúc đẩy huyết khối trên bề mặt nội mạc tiểu nhĩ, bên cạnh hoạt hóa tiểu cầu và các tế bào viêm, cũng như bổ xung vào trạng thái thúc đẩy huyết khối nói chung. Hoạt hóa hệ thống đông máu nhĩ và hệ thống có thể giải thích một phần vì sao các cơn AF ngắn đưa đến nguy cơ đột quỵ kéo dài.
Theo timmachhoc.vn
PK Đức Tín
Tin tức liên quan
Điện thoại bàn: (028) 3981 2678
Di động: 0903 839 878 - 0909 384 389