Ảnh hưởng của ức chếmen chuyển lên tiêu sợi huyết được chứng minh trong một nghiên cứu gồm 16 người lớn có huyết áp bình thường được truyền bradykinin vào động mạch cánh tay. Sựphóng thích t-PA hoạt hóa từnội mô sau đáp ứng kích thích tại chỗcủa bradykinin tăng lên hơn gấp đôi khi được điều trịquinapril so với được điều trịbằng giảdược hoặc losartan. Tương tựtrong một nghiên cứu ởnhững bệnh nhân suy tim có triệu chứng, liệu pháp ức chếmen chuyển gây tăng phóng thích t-PA tại chỗsau khi truyền bradykinin vào động mạch cánh tay
Tác dụng này bịloại bỏbởi HOE 140, mà không phải chất đối kháng B1R [84]. Tác dụng nhóm cũng đã chứng minh khi điều trịnhững bệnh nhân đái tháo đường có tăng huyết áp với perindopril giúp làm giảm mức PAI-1 huyết tương. Giảm PAI-1 không thấy ởlosartan mặc dù có mức hạhuyết áp tương tự, hiệu quảnày do ảnh hưởng thông qua tác động của bradykinin hơn là tác động của Angio I/Angio II.
Mô hình thực nghiệm ởđộng vật có tăng huyết áp và bệnh lý tim mạch đã giúp củng cốcác phát hiện lâm sàng này. Trong một nghiên cứu ởnhững con chuột tăng huyết áp tự nhiên, khi sửdụng HOE 140 làm mất đi khảnăng gây tăng tạo GMP vòng ởđộng mạch chủ, một chất có tác dụng gây dãn mạch, do tác động của ramipril và perindopril. Ởchuột B1R -/-/B2R -/-, việc điều trịbằng captopril giúp làm giảm hoạt động kênh sodium thượng bì mạnh hơn đáng kểkhi so với ởchuột hoang. Ởchuột Wistar có đái tháo đường khi điều trịbằng perindopril hoặc ramipril giúp làm giảm tăng huyết áp và trọng lượng mạch máu mạc treo ruột và tỉlệlớp áo giữa: diện tích lồng ống mạch. Dùng đồng thời chất đối kháng HOE 140 của B2R tiêm dưới da làm mất đi tác dụng của các thuốc ức chếmen chuyển lên trọng lượng mạch và tỉlệlớp áo giữa: diện tích lòng mạch. Tương tựởchuột có đái tháo đường khi sửdụng ramipril giúp ngăn chặn albumin niệu và xơ hóa cầu thận. HOE 140 làm mất đi các tác dụng này.
Ức chếmen chuyển thông qua thụthểB1R mang đến những lợi ích khác. Trong thửnghiệm EUROPA gồm những bệnh nhân với bệnh mạch vành ổn định, sựđa dạng kiểu hình của B1R có liên quan đến việc làm giảm kết cục chính (tửvong do nguyên nhân tim mạch, nhồi máu cơ tim không tửvong, và ngưng tim được cứu sống) khi được điều trịvới perindopril 10 mg [91]. Ức chếmen chuyển giúp hoạt hóa B1R cũng được chứng minh ởnội mô [22,92]. Một nghiên cứu trên động mạch vành của bò bị co thắt từ trước cho thấy điều trịcaptopril giúp tăng cường mức dãn mạch thông qua bradykinin, hiệu quảnày bịức chếbởi chất NOS và chất đối kháng B1R, không phải chất đối kháng B2R. Hơn nữa việc điều trịvới enaprilat giúp tăng hoạt hóa trực tiếp B1R, dẫn đến tăng phóng thích NO ởtếbào nội mô [93]. Một sốức chếmen chuyển hoạt động như đồng vận trực tiếp của B1R.
Nhiều điều chưa được hiểu hết vềvai trò của B2R và B1R trong những giai đoạn bệnh khác nhau. Trong mô hình thiếu máu cục bộ cơ tim ởchuột, ramipril và đồng vận B2R làm giảm kích thước mảng nhồi máu đáng kể, nhưng đồng vận B1R Des-Arg(9)-BK thì không có hiệu quảnày. Tuy nhiên ởmô hình thực nghiệm chuột có đái tháo đường, không phải ramiprilat cũng không phải đồng vận B2R làm giảm kích thước mảng nhồi máu, mà là Des-Arg(9)-BK làm giảm 44% kích thước mảng nhồi máu [28]. Những dữliệu rồi cho thấy sựphức tạp của B2R/B1R và nhấn mạnh vai trò của bradykinin trong việc bảo vệ tim mạch thông qua tác dụng của thuốc ức chếmen chuyển.
Cuối cùng, B2R tăng mức biểu thịởngười trẻ, vì vậy những bệnh nhân trẻsẽhưởng lợi nhiều hơn khi được sửdụng ức chếmen chuyển trong điều trị, tăng mức bradykinin sinh khảdụng sẽgiúp tăng kích thích các thụthểtựdo. Ý kiến này giống với dữliệu được công bốtrong thửnghiệm phân tích gộp năm 2009 của Brugts và cộng sự[85], bao gồm 29.000 bệnh nhân từcác nghiên cứu EUROPA, ADVANCE và PROGRESS. Mặc dù giảm được 18% kết cục các biến cốtim mạch và tửvong trên dân sốchung, nhưng những bệnh nhân dưới 60 tuổi đạt được nhiều lợi ích hơn khi được điều trịvới perindopril, phần lớn được sửdụng liều 10 mg (hình 4). Hơn nữa, trong mô hình tiền lâm sàng chuột có tăng huyết áp, việc sửdụng perindopril thời gian ngắn khi bắt đầu có tăng huyết áp giúp ngăn ngừa sựtăng huyết áp do lão hóa [94]. Những dữliệu này ủng hộý kiến cho rằng các thuốc ức chếmen chuyển có hiệu quảbảo vệmạch máu nhiều hơn ởngười trẻvà khảnăng làm chậm sựtiến triển của bệnh lý tim mạch khi được sửdụng sớm sau chẩn đoán tăng huyết áp.
4.1.Sựkhác biệt giữa các thuốc ức chếmen chuyển
Các thuốc ức chếmen chuyển được phân thành ba nhóm dựa trên nhóm gắn kết chức năng: captopril và zofenopril có chứa gốc sulfhydryl; benazepril, enalapril, lisinopril, perindopril, quinapril, Ramipril, và trandolapril chứa gốc dicarboxylate; và fosinopril chứa gốc phosphonate [95]. Sựkhác biệt vềcấu trúc này ảnh hưởng đến dược động và dược lực của thuốc. Vịtrí gắn kết của ức chếmen chuyển có ảnh hưởng đến hiệu quảthuốc thông qua bradykinin và Angio-I. Trong thửnghiệm vềmức gắn kết in vitro sửdụng tếbào nội mô người, tỉlệchọn lọc gắn kết bradykinin/Ang I là 1.44 đối với perindopril, 1,16 đối với ramiprilat, 1,09 đối với quinaprilat, 1,08 đối với trandoprilat, và 1.00 đối với enaprilat. Dữliệu cho thấy so với các thuốc ức chếmen chuyển khác, perindopril có tính chọn lọc trên bradykinin nhiều hơntrên Ang I [14]. Các thuốc ức chếmen chuyển cũng có mức gắn kết với mô tim khác nhau, cao nhất là perindopril, theo sau là quinalaprilat, ramiprilat, kếđó là enalaprilat và fosinoprilat, và sau cùng là captopril.
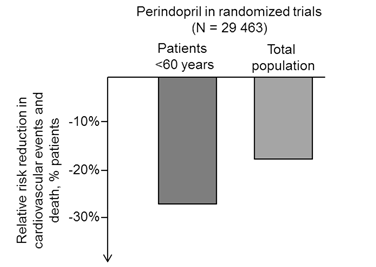
Hình 4: Ảnh hưởng có liên quan đến tuổi của thuốc ức chếmen chuyển perindopril giúp làm giảm tửvong và các biến cốtim mạch trong các thửnghiệm lâm sàng. Trong phân tích gộp từcác thửnghiệm EUROPA, ADVANCE, và PROGRESS, perindopril giúp làm giảm nguy cơ tương đối các biến cốtim mạch và tửvong nổi bật ởnhóm bệnh nhân trẻ(< 60 tuổi) so với nhóm dân sốchung. Sựkhác biệt này được giải thích do mức bradykinin có chức năng ởngười trẻnhiều hơn [85].
Sựkhác biệt vềvai trò sinh học quan trọng của bradykinin chưa được hiểu đầy đủ. Nhờvào sựkết hợp tính ái mỡ, gắn kết cao với mô, và có tỉlệchọn lọc bradykinin/Ang I cao perindopril cho hiệu quảức chếchuyển hóa bradykinin kéo dài hơn, hoàn toàn hơn và do đó tăng hiệu ứng sinh học hơn so với các thuốc ức chế men chuyển khác. Ít nhấtmột nghiên cứu đối đầu đã ủng hộgiảthuyết này và chứng minh các thuốc ức chếmen chuyển có ảnh hưởng khác biệt trên chết tếbào nội mô theo chương trình phản ánh sựkhác biệt trong tỉlệchọn lọc bradykinin/Ang I [14,97]. Khi sửdụng các thuốc ức chế men chuyển cho chuột trong khoảng thời gian 7 ngày với liều hiệu quảhạáp giống nhaugiúp giảm tỉlệchết tếbào nội mô theo chương trình thông qua lipopolysaccharide. So với chất nghiên cứu, perindopril làm giảm hiệu quảkhác biệt có ý nghĩa thống kê (p < 0,001), hiệu quảnày không thấy với các thuốc ức chếmen chuyển khác. Thứtựđộmạnh trong thực nghiệm này là perindopril >ramipril >> quinapril = trandolapril = enalapril. Sựkhác biệt giữa các thuốc ức chếmen chuyểncó ý nghĩa khi so perindopril với quinapril (p < 0,01), perindopril với trandolapril (p < 0,001), và perindopril với enalapril (p < 0,001) [97]. Dữliệu này cho thấy perindopril có hiệu quảcao trên nội mô, tương tựvới thửnghiệm PERTINENT, báo cáo giảm 31% chết tếbào theo chương trình ởtếbào nội mô người, và gợi ý perindopril có khảnăng bảo tồn bradykinin cao ởnội mô [76].
4.2.Vai trò của bradykinin trong đáp ứng liều đối với các ức chếhệthống Renin-Angiotensin
Một bài báo được công bốgần đây trình bày các bằng chứng cho thấynhững khác biệt phụthuộc liều giữa các thuốc ức chếmen chuyển và ARB [98]. Những yếu tố này đặc biệt thú vị để thảo luận trong bối cảnh hiểu biết của chúng ta về bradykinin.
Vềkhía cạnh giảm huyết áp, thuốc ức chếmen chuyển perindopril được chứng minh trong nhiều nghiên cứu có khảnăng làm giảm thêm huyết áp khi tăng từ5 mg lên 10 mg. Trong nghiên cứu Confidence [99], perindopril được tăng liều từ5 mg lên 10 mg sau 2 tuần (N= 1943 và mức huyết áp tâm thu trung bình là 154,5 mmHg), SBP giảm -8 mmHg sau 2 tuần và giảm -18 mmHg sau 12 tuần điều trị(p so với ban đầu < 0,01). Mức giảm huyết áp đáng kểthấy ở193 bệnh nhân có tăng huyết áp nặng lúc ban đầu (mức huyết áp tâm thu trung bình ban đầulà 182,4 mmHg). SBP giảm -23 mmHg với perindopril 5 mg (đo ởtuần thứ2) và giảm -38 mmHg với perindopril 10 mg (đo ởtuần 12). Trong một nghiên cứu gần đây [100], gồm 1004 bệnh nhân tăng huyết áp độ1 và độ2 (mức trung bình SBP/DBP là 155,8/92,8 mmHg), được điều trịvới perindopril 5 mg giảm huyết áp trung bình 9,6/5 mmHg trong 2 tuần, trong khi đó những bệnh nhân được sửdụng perindopril 10 mmHg có mức giảm huyết áp trung bình 18,1/9,5 mmHg. Hiệu quảgiảm huyết áp phụthuộc liều không thấy với ARB. Thật vậy, các ức chếRAS có xu hướng giảm giảm huyết áp nhanh vì nó ngăn chặn việc gắn kết Ang II có tác dụng gây co mạch với thụthểAT1. Tuy nhiên, hiệu quảnày nhanh chóng bịbão hòa, ARB có đường cong đáp ứng liều dạng lõm không sâu, và không có lợi ích lên hiệu quảgiảm huyết áp khi tăng liều từ50% lên 100% [101]. Hơn nữa, cơ chếtác động trực tiếp của ARB có nguy cơ cao hơn gây ra các cơn tụt huyết áp thoáng qua [102]. Xem xét 16 thửnghiệm gồm hơn 113.000 bệnh nhân, việc sửdụng ARB làm tăng nguy cơ tụt huyết áp 56% (p< 0,001). Các tác giảđồng ý với tác dụng phụbất lợi này như là sựgiải thích cho việc tăng tửvong chung do mọi nguyên nhân (+3;p= 0,05) được báo cáo trong nghiên cứu.
Thật vậy, từcơ chếhoạt động mà hiệu quảphụthuộc liều của ARB khá hạn chế. Hoạt động của các ARB dựa trên mức giảm của đường chuyển hóa Ang. Một khi sựbão hòa dược học và sựức chếtoàn phần xảy ra, mức giảm Ang không thểxảy ra hơn nữa và sựtăng liều không có ý nghĩa. Mặc dù tất cảcác thuốc ức chế RAS đều có đặc tính này, các thuốc ức chếmen chuyển làm tăng sinh khảdụng của bradykinin. Nghiên cứu tiền lâm sàng của Cambell và cộng sự[77] đã chứng minh với liều thấp của perindopril, tỉlệAng II/Ang I giảm một cách đáng kể. Tuy nhiên việc tăng bradykinin huyết tương gần như tuyến tính với việc tăng liều perindopril. Do đó, với các ức chếACE, hoạt động bradykinin trởnên ưu thếkhi lợi ích của sựgiảm Ang II bịbão hòa. Hình 5 tóm tắt lại sựkhác biệt mô hình hoạt động của các thuốc ức chếmen chuyển và ARB.
Trong thực hành lâm sàng, sựkhác biệt vềhiệu quảcủa các thuốc ức chếmen chuyển lên Ang II và bradykinin đã được ghi nhận một thời gian dài trước đây. Năm 1986 trong một nghiên cứu trên 18 người đàn ông có huyết áp bình thường, việc ức chếkhảnăng hoạt động của ACE trong huyết tương đểtạo ra Ang II bão hòa, dạng bình nguyên, khi đạt đến liều 10 mg với tỉlệức chếlà 80, 84, 95, và 96% với liều perindopril tương đương là 2,5–5– 10 và 20 mg [103]. Ngược lại, một thửnghiệm ngẫu nhiên, mù đôi chưa được công bốtrước đó được thực hiện ởHeidelberg Australia trên 12 người lớn trưởng thành khỏe mạnh có huyết áp bình thường, khoảng dưới đường cong kéo dài hơn 48 giờchứng tỏmức bradykinin huyết tương khi tăng liều perindopril (Hình 6) . Không có sựbão hòa rõ ràng thấy được ngay cảkhi liều perindopril cao hơn được dùng trong các thực nghiệm lâm sàng. Những bệnh nhân này có tuổi đời trung bình là 27 ±2,8 và cân nặng 72,8 ± 3,5 kg, có mức huyết áp ban đầu SBP/DBP là 124,8 ± 2,2 mmHg, và được sửdụng perindopril liều uống 5, 10, và 20 mg hoặc giảdược ởcác khoảng cách thời gian 7 ngày.
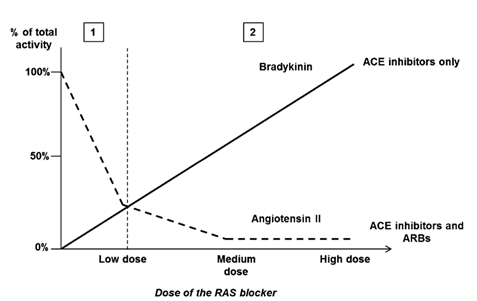
Hình 5: Mô hình dựđoán ảnh hưởng của bradykinin và angiotensin II lên hiệu quảphụthuộc liều của các thuốc ức chếRAS.Ởliều tương đối thấp (1), các thuốc ức chếmen chuyển và ARB làm giảm hoạt tính của angiotensin II. Hiệu quảnày nhanh chóng bịbão hòa. Ởliều cao (2), các thuốc ức chếmen chuyển giúp bảo tồn bradykinin tránh bịthoái gián. ACE angiotensin converting enzyme, ARB angiotensin receptor blocker, RAS renin-angiotensin system
Theo timmachhoc.vn
PK Đức Tín
Tin tức liên quan
Điện thoại bàn: (028) 3981 2678
Di động: 0903 839 878 - 0909 384 389